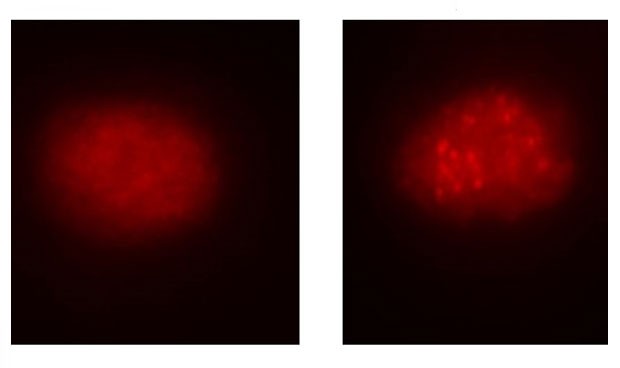
A la izquierda, célula de un paciente con anemia de Fanconi antes de la corrección. A la derecha, la célula ya corregida.
La progresión en el tratamiento de la
anemia de Fanconi, una enfermedad de origen genético y baja prevalencia (un caso por cada 160.000 habitantes), parece imparable en los últimos tiempos.
Un
ensayo clínico demostró que las células madre reparadas del defecto en uno de los genes afectados y reintroducidas en el paciente tenían
efectos positivos estables. Ahora, se ha demostrado que es sencillo ‘arreglar’ esas células madre gracias a la herramienta de edición genética
Crispr/Cas9.
Se trata de una investigación preclínica que se propone como una estrategia de tratamiento tanto para la anemia de Fanconi como para otras enfermedades que afectan a las
células madre de la sangre por su simplicidad y gran eficacia, “sobre todo fallos de
médula ósea que se comportan de forma parecida a Fanconi”, comenta
Paula Río, de la división de
Terapias Innovadoras del Centro de Investigaciones Energéticas, Medioambientales y Tecnológicas (
Ciemat), que ha participado en el estudio.
Unión de extremos no homólogos
Hasta ahora, se había utilizado la recombinación homóloga, es decir, sustituir el gen afectado por otro sano mediante el uso de
vectores lentivirales. La aproximación actual busca corregir los puntos de la secuencia que han mutado, algo similar al mecanismo de reparación de las propias células y que, por tanto, tiene una mayor tasa de éxito.
|
Río: "Por lo que hemos visto en laboratorio, la posibilidad de que Crispr reconozca otras regiones es muy baja si está bien diseñada la secuencia"
|
“Ya habíamos visto en otro trabajo que en estos pacientes la reparación mediante recombinación homóloga la tienen defectuosa”, explica Río. Por tanto, la reparación puntual, llamada unión de extremos no homólogos, logra una tasa mayor de éxito. “
Podemos llegar a eficacias de corrección del 30 por ciento, suficiente para cualquier enfermedad”.
Complicaciones del trasplante
Las mutaciones que dan origen a la anemia de Fanconi provocan un fallo de la médula ósea que
genera células sanguíneas deficientes desde edades muy tempranas. El trasplante de progenitores hematopoyéticos es la terapia de elección, pero no todos los pacientes tienen un donante adecuado, además de poder sufrir rechazos. La corrección de células madre del propio paciente evita estas complicaciones.
Río afirma que se han corregido mutaciones en el gen “Fanconi A y en otros como Fanconi C, B y BRCA2. No se puede utilizar para todas las mutaciones, pero
alrededor de un 40 por ciento de ellas pueden corregirse mediante esta aproximación”.
Mutaciones no deseadas
Crispr es una tecnología que ha cambiado el panorama de la edición genética, pero sobre la que todavía hay
suspicacias a la hora de aplicar en terapias clínicas pues se desconocen los efectos a largo plazo y se teme que provoque mutaciones indeseadas. No obstante, Río afirma que “hemos analizado la posibilidad de que una de las Crispr se pueda dirigir a otros sitios del genoma:
lo hemos hecho en 20 sitios diferentes y hemos visto que no ocurre”.
Y continúa: “Esto se decía en los primeros estudios, y todavía en pacientes hay que demostrarlo, pero por lo que hemos visto en laboratorio, la posibilidad de que reconozca otra región es muy baja si está bien diseñada la secuencia, esto ha mejorado mucho”.
Número suficiente de células
El siguiente paso tras esta prueba es hacer un estudio a gran escala, con un número mayor de células, “para optimizar el paso a la clínica.
Este mes vamos a recibir la máquina que nos permita este paso”, indica la investigadora, que, si todo va bien, considera que “en cinco o seis años” se podrá empezar a utilizar esta aproximación en los tratamientos convencionales.
El estudio, publicado en Cell Stem Cell, ha sido realizado por personal del Centro de Investigaciones Energéticas, Medioambientales y Tecnológicas (Ciemat), el Centro de Investigacióni Biomédica en Red de Enfermedades Raras (Ciberer) y el Instituto de Investigación Sanitaria de la Fundación Jiménez Díaz (IIS-FJD), dirigidos por Río. El primer firmante del trabajo es Francisco José Román-Rodríguez.
Las informaciones publicadas en Redacción Médica contienen afirmaciones, datos y declaraciones procedentes de instituciones oficiales y profesionales sanitarios. No obstante, ante cualquier duda relacionada con su salud, consulte con su especialista sanitario correspondiente.