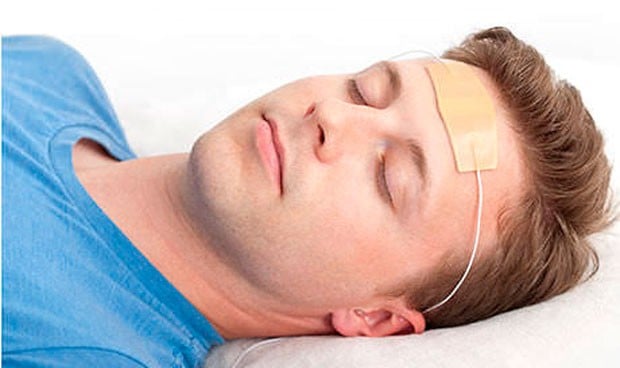
Se conecta a través de un cable a un pequeño parche que se adhiere a la frente del paciente.
La agencia estadounidense encargada de la administración de alimentos y medicamentos (FDA, por sus siglas en inglés) ha otorgado a NeuroSigma la
comercialización del primer dispositivo médico para tratar el trastorno por déficit de atención e hiperactividad (TDAH). El dispositivo de venta con receta, denominado
sistema de estimulación externa del nervio trigémino (eTNS) de Monarch, está indicado para pacientes de
siete a 12 años que actualmente no toman medicamentos recetados para tratar la enfermedad.
El sistema Monarch eTNS está diseñado para ser
utilizado en el hogar durante los periodos de sueño y bajo la
supervisión de un cuidador. El dispositivo, del
tamaño de un teléfono móvil, genera un pulso eléctrico de bajo nivel y se conecta a través de un cable a un
pequeño parche que se adhiere a la frente del paciente, justo por encima de las cejas, y debe sentirse como una
sensación de hormigueo en la piel. El sistema entrega la estimulación eléctrica de bajo nivel a las ramas del nervio trigémino, que envía señales terapéuticas a las partes del cerebro que se cree que están involucradas en el TDAH.
|
El sistema aumenta la actividad en las regiones del cerebro importantes para regular la atención, emoción y comportamiento
|
Si bien aún no se conoce el mecanismo exacto de eTNS, los estudios de neuroimagen han demostrado que
aumenta la actividad en las regiones del cerebro que se sabe que son importantes para regular la atención, la emoción y el comportamiento. Los ensayos clínicos sugieren que una respuesta a eTNS puede tardar hasta cuatro semanas en hacerse evidente.
Se trata del
primer tratamiento no farmacológico para el TDAH con autorización de comercialización otorgada por la FDA. Carlos Peña, Ph.D., director de la División de Neurología y Dispositivos de medicina física en el Centro de dispositivos y salud radiológica de la FDA, ha asegurado que este nuevo dispositivo ofrece una "
opción segura mediante el uso de estimulación nerviosa leve, una de sus características".
Mejoría significativa de los síntomas
La eficacia del Sistema eTNS en el tratamiento del TDAH se demostró en un ensayo clínico que comparó el sistema como el único tratamiento, o monoterapia, con un dispositivo placebo. Un total de 62 niños con TDAH moderado a grave se inscribieron en el ensayo y utilizaron esta terapia cada noche o un dispositivo de placebo en el hogar durante cuatro semanas. El ensayo mostró que los sujetos que utilizaron eTNS tuvieron una
mejoría estadísticamente significativa en sus síntomas de TDAH en comparación con el grupo de placebo.
Los efectos secundarios más comunes observados con el uso de eTNS son somnolencia, aumento del apetito, dificultad para dormir, dolor de cabeza y fatiga. Por otro lado,
no se asociaron eventos adversos graves con el uso del dispositivo.
Las informaciones publicadas en Redacción Médica contienen afirmaciones, datos y declaraciones procedentes de instituciones oficiales y profesionales sanitarios. No obstante, ante cualquier duda relacionada con su salud, consulte con su especialista sanitario correspondiente.